|
| Firmenprofil |
| Leistungen |
| Referenzen |
| Veröffentlichungen |
| Kontakt |
| Impressum |

UV-Naßoxidationsverfahren
|
Das Naßoxidatinsverfahren schließt eine Lücke
bei der Abwasserbehandlung. Die Zerstörung
einiger bisher nur sehr schwierig oder gar
nicht behandelbarer Abwasserinhaltsstoffe
werden durch Naßoxidation zu ungefährlichen
Produkten ohne weitere chemische
Umweltbelastung. Oxidation und Oxidationsmittel Vorteile, Nachteile und Risiken:Die Oxidation ist einer der wichtigsten Prozesse zur Abwasserbehandlung. Sie ist der Entzug von Elektronen bei dem zu oxidierenden Stoff, der in vielen Fällen durch die Aufnahme von Sauerstoff begleitet wird. Dieser Vorgang wird zur Entgiftung gefährlicher Stoffe wie Cyanid und Nitrit und zum Abbau organischer Substanzen, die durch CSB oder BSB erfaßt werden, benutzt. Für alle diese Reaktionen lassen sich Oxidationsmittel wie z. B. Chlor, Hypochlorit, Wasserstoffperoxid, Caroat, Persulfat, Kaliumpermanganat, Ozon oder auch Sauerstoff einsetzen. Chlor und chlorabspaltende Verbindungen haben den Nachteil, daß sie anwesende organische Verbindungen chlorieren und damit zur Bildung von adsorbierbaren organischen Halogenverbindungen (AOX), also zu gefährlichen und im Abwasser limitierten Stoffen führen. Chromat und (Per)Manganat enthalten selbst gefährliche Stoffe und/oder führen durch die Abtrennung ihrer Reaktionsprodukte zu erhöhtem Abfall (Schlamm). |
Ozon, Caroat und Persulfat sind kostspielige
Oxidationsmittel oder führen zu betonagressiven
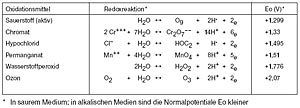
Sulfatreaktionen. Die verbleibenden Oxidantien Wasserstoffperoxid und Sauerstoff sind zusammen mit dem Ozon sehr umweltfreundlich, da sie keinen Beitrag zu einer Aufsalzung der zu behandelten Lösung liefern. Sauerstoff reagiert aber nur in aktiviertem bzw. atomarem Zustand in gewünschter Weise, den er nur sehr kurzfristig beibehält. Stärke der Oxidationsmittel Ausschlaggebend für eine Oxidation ist, wie leicht oder wie schwer sich ein Stoff oxidieren läßt und wie stark ein Oxidationsmittel wirkt. Je höher das sogenannte Normalpotential eines Stoffes ist, umso stärker ist seine oxidierende Wirkung. Die Tabelle unten enthält die Redox-Reaktionen von Sauerstoff und seinen Verbindungen in der Reihenfolge steigender Potentiale.Das Oxidationsmittel des Naßoxidationsverfahrens das Hydroxilradikal hat sowohl im sauren Bereich (+2,8 V) als auch im alkalischen Bereich (+2,0 V) das positivste Normalpotential aller Oxidationsmittel. Alle Stoffe, deren Normalpotentiale negativer sind als eines in der Tabelle angeführten, lassen sich von dem Stoff mit dem positiveren Normalpotential oxidieren.
|
|||||||||||||||||||||||
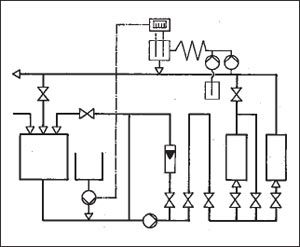
Prinzip des Naßoxidationsverfahrens
|
Erzeugung von Hydroxylradikalen durch UV-Licht Hydroxylradikale bilden sich bei Einfluß von ultravioletten Strahlen auf Wasserstoffperoxid. Das Wasserstoffperoxidmolekül teilt sich in zwei OH-Radikale: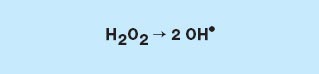
Erst nach Bildung der OH-Radikale erfolgt die Oxidation. Die sehr unbeständigen, reaktionsfreudigen Radikale mit der hohen Sauerstoffüberbilanz reagieren sofort mit allen oxidierbaren Stoffen, mit denen sie zusammentreffen. Reaktionsprodukte sind: Kohlensäure, Wasser, Nitrat, Sulfat, Chlorid, z. B. bei der Reaktion mit Tetrachlorethen: 
Die Oxidation nach dem Naßoxidationsverfahren setzt sich also aus 2 Teilreaktionen zusammen: 1. Fotoreaktion zur Bildung von OH-Radikalen 2. Chemische Oxidation eines oxidierbaren Substrats Beide Reaktionen verlaufen in homogener Phase, so daß die Nachteile der Reaktionen an Phasengrenzflächen, die bei der anodischen Oxidation und bei der Ozonreaktion zwangsweise auftreten, mit denen ihnen eigenen Erschwernissen ausgeschlossen sind. |
Einsatzmöglichkeiten des Naßoxidationsverfahrens
|
||||||||||||||||||||||||||||||||||||||||||||
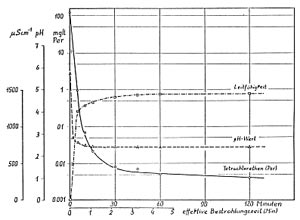
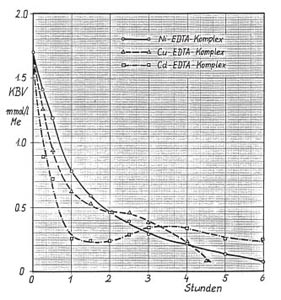
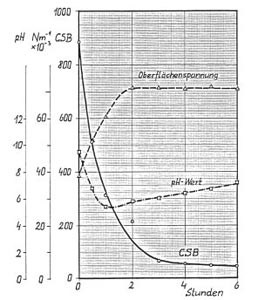
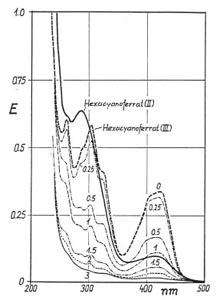
Einige Behandlungsergebnisse, die durch die UV-Oxidationsverfahren
ermittelt wurden und die Einsatzmöglichkeiten des Verfahrens aufzeigen.
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||